바턴-켈로그 반응
| 바턴-켈로그 반응 | |
|---|---|
| 이름이 붙여진 대상 | 디릭 바턴 경 리처드 M. 켈로그 |
| 반응 유형 | 짝지음 반응 |
| 식별자 | |
| RSC ontology ID | RXNO:0000495 |
바턴-켈로그 반응(영어: Barton–Kellogg reaction)은 다이아조 화합물과 티오케톤 사이에서 에피설파이드 중간체를 거쳐 알켄을 생성하는 짝지음 반응이다.[1][2][3] 바턴-켈로그 반응은 바턴-켈로그 올레핀화(영어: Barton–Kellogg olefination)[4] 및 바턴 올레핀 합성(영어: Barton olefin synthesis)이라고도 알려져 있다.[5]

이 반응은 헤르만 슈타우딩거가 개척했으며[6], 슈타우딩거형 다이아조-티오케톤 짝지음(영어: Staudinger type diazo-thioketone coupling)이라는 이름으로도 불린다.
반응 과정
[편집]이 반응의 반응 과정에서 다이아조 화합물은 티오케톤과 1,3-쌍극자 고리화 첨가 반응에서 1,3-쌍극자로 반응하여 5원자 싸이아다이아졸린 고리를 형성한다. 이 중간체는 불안정하며, 질소 분자를 내보내 티오카보닐 일라이드를 형성한 다음 고리화되어 안정한 에피설파이드를 형성한다. 트라이페닐포스핀은 친핵체로 반응하여 3원자 고리를 열어 설파포스파테인을 형성한다. 비티히 반응과 유사한 방식으로 이 구조는 트라이페닐포스핀 설파이드를 방출하여 알켄을 생성한다.

범위
[편집]다이아조 화합물은 하이드라진과 반응하여 하이드라존을 거쳐 산화함으로써 케톤으로부터 얻을 수 있다. 이러한 전환을 위한 많은 시약이 존재하는데, 예를 들어 산화 은(I)과 (비스(트라이플루오로아세톡시)아이오도)벤젠 등이 있다.[7] 이 반응에 필요한 티오케톤은 케톤과 오황화 인으로부터 얻을 수 있다. 에피설파이드의 탈황은 많은 포스핀과 구리 분말에 의해 수행될 수 있다.
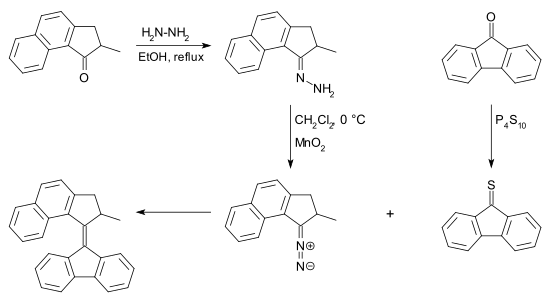
이 반응이 맥머리 반응보다 갖는 주요 장점은 두 가지 다른 케톤을 가지고 반응이 일어날 수 있다는 점이다. 이러한 점에서 다이아조-티오케톤 짝지음은 동종 짝지음이 아니라 교차 짝지음이다.
각주
[편집]- ^ D. H. R. Barton; B. J. Willis (1970). 《Olefin synthesis by twofold extrusion processes》. 《J. Chem. Soc. D》. 1225쪽. doi:10.1039/C29700001225.
- ^ R. M. Kellogg; S. Wassenaar (1970). 《Thiocarbonyl ylides. An approach to "tetravalent sulfur" compounds》. 《Tetrahedron Lett.》 11. 1987쪽. doi:10.1016/S0040-4039(01)98134-1.
- ^ R. M. Kellogg (1976). 《The molecules R2CXCR2 including azomethine, carbonyl and thiocarbonyl ylides. Their syntheses, properties and reactions》. 《Tetrahedron》 32. 2165–2184쪽. doi:10.1016/0040-4020(76)85131-9.
- ^ 〈Barton-Kellogg olefination〉. 《Comprehensive Organic Name Reactions and Reagents》. 2010. 249–253쪽. doi:10.1002/9780470638859.conrr056. ISBN 9780470638859.
- ^ 〈Barton olefin synthesis〉 15판. 《Merck Index》.
- ^ H. Staudinger; J. Siegwart (1920). 《Einwirkungen von aliphatischen Diazoverbindungen auf Thioketone》. 《Helv. Chim. Acta》 3. 833–840쪽. doi:10.1002/hlca.19200030178.
- ^ Matthijs K. J. ter Wiel; Javier Vicario; Stephen G. Davey; Auke Meetsma; Ben L. Feringa (2005). 《New procedure for the preparation of highly sterically hindered alkenes using a hypervalent iodine reagent》 (PDF). 《Organic & Biomolecular Chemistry》 3. 28–30쪽. doi:10.1039/b414959a. PMID 15602594.
