Structuurformule
Een structuurformule is een chemische formule die in meer of mindere mate weergeeft hoe de atomen in een molecuul met elkaar zijn verbonden en hoe zij ruimtelijk zijn georganiseerd.[1][2][3] Een structuurformule geeft meer informatie dan een molecuulformule, die alleen de aantallen atomen in een molecuul weergeeft of een verhoudingsformule met alleen de verhoudingen in een stof tussen de verschillende atomen.
Structuurformules komen in veel gedaanten voor. In de eenvoudigste gevallen wordt de structuur kenbaar gemaakt door de volgorde van de symbolen van de elementen en met behulp van haakjes. De structuur is af te leiden uit de formule maar niet letterlijk zichtbaar. Men spreekt ook van gecondenseerde structuurformules.
Voorbeelden:
- HCNO (fulminezuur) en HNCO (isocyaanzuur), beide met molecuulformule CHNO. De volgorde van de symbolen in de structuurformule toont in welke volgorde de atomen zijn verbonden.
- Pb(C2H5)4 (tetra-ethyllood), met molecuulformule C8H20Pb. De structuurformule toont dat het om een vier ethylgroepen gaat gebonden op een loodatoom.
- Na2SO4·10H2O (natriumsulfaatdecahydraat), met verhoudingsformule H20Na2O14S. Men leest in de structuurformule dat het een ionaire verbinding tussen natrium(1+) en sulfaat betreft, waarbij er per Na2SO4-eenheid tien watermoleculen in het kristal aanwezig zijn.
De structuurformule kan ook een grafische weergave van de structuur zijn en elke chemische binding weergeven. Deze formules kunnen meer gedetailleerde informatie bevatten over de structuur, bijvoorbeeld door het weergeven van dubbele en drievoudige bindingen en vrije elektronenparen en van de stereochemie en de conformatie. De driedimensionale structuur wordt verduidelijkt door het gebruik van perspectief of door specifieke projecties, zoals de fischer- en haworthprojectie. In de organische chemie zijn de skeletstructuren de meest gebruikte structuurformules.
Voorbeelden:
- Propaan. De structuurformule toont alle atomen en alle bindingen.
- Siliciumdioxide. De structuurformule toont hoe het covalente netwerk is opgebouwd.
- Azijnzuur: de structuurformule toont het type binding en de vrije elektronenparen.
- Lysergeenzuurdi-ethylamide: De structuurformule is tot een skeletstructuur geabstraheerd.
- Sulfaat: De driedimensionale structuur is in perspectief weergegeven.
- D-sorbitol: De stereochemie is met de fischerprojectie weergegeven.
Voor veel organische moleculen volstaat een structuurformule die de verschillende atomen en de bindingen ertussen tweedimensionaal weergeeft. Bij andere stoffen zijn meer symbolen nodig om ze bruikbaar weer te geven. Dat is bijvoorbeeld het geval voor aromatische moleculen, andere resonante structuren, complexen en ionen. Structuurformules volgen uit de lewistheorie en -notatie voor binding. Hoewel vrije elektronenparen vaak niet in structuurformules worden weergegeven, kan dat wel. Structuurformules waarin ook de vrije elektronenparen staan zijn lewisstructuren.
Onderdelen van een structuurformule
[bewerken | brontekst bewerken]Een molecuul is een fysisch gegeven en kan met de daarvoor geschikte techniek worden waargenomen. Een structuurformule is een poging tot een bruikbare weergave op papier van de belangrijkste kenmerken van een molecuul.
- De letters staan voor de atoomkernen.
- De streepjes staan voor bindingen tussen atomen, maar kuunen net zoals dubbele stippen vrije elektronenparen aangeven.
Ieder streepje geeft twee valentie-elektronen weer. Dat zijn elektronen van de buitenste schil, van de valentieschil. Een streepje kan zowel een binding tussen twee atomen voorstellen als een vrij elektronenpaar. Een vrij elektronenpaar hoort bij een atoom en maakt geen deel uit van een binding.
Een formele lading is een lading zoals ze voorkomt in een structuurformule. Het is de uitdrukking van de elektrische lading van een atoom in een structuurformule. De formele lading hangt af van het aantal negatieve ladingen, dus van het aantal elektronen en van het aantal positieve ladingen, van het aantal protonen. Van de atomen kunnen alleen de valentie-elektronen worden opgenomen of afgegeven. Het aantal protonen in de atoomkern van de elementen in een chemische reactie verandert nooit.
Concreet
[bewerken | brontekst bewerken]In principe geeft de structuurformule van een stof aan:
- welke atomen er in de stof aanwezig zijn,
- welke atomen er aan elkaar gebonden zijn,
- met hoeveel bindingselektronenparen twee atomen aan elkaar zijn gebonden,
- dat het om een enkele, dubbele of drievoudige binding gaat,
- welke atomen vrije elektronenparen dragen,
- welke atomen formele ladingen dragen en
- welke hoeken de bindingen met elkaar maken, alleen in beperkte zin.
In de praktijk komt het voor dat in de structuurformule
- de koolstof- en waterstofatomen niet allemaal worden weergegeven,
- de enkele bindingen niet expliciet worden geschreven,
- de vrije elektronenparen niet altijd worden aangebracht en
- met de bindingshoeken helemaal geen rekening wordt gehouden.
Isomeren
[bewerken | brontekst bewerken]Chemische verbindingen kunnen in verschillende geometrische (ruimtelijke) vormen voorkomen. De structuurformule geeft de ruimtelijke rangschikking van de atomen weer, wat in een molecuulformule (of brutoformule) niet kan.
Een van de voordelen van een structuurformule is de mogelijkheid van de weergave van isomeren.
Voorbeelden:
- Butaan, molecuulformule C4H10. De vier koolstofatomen in butaan zijn lineair gerangschikt, ze liggen op één lijn. In isobutaan (methylpropaan) daarentegen liggen de vier koolstofatomen als een T vertakt.
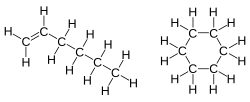
- Molecuulformule: C6H12. hex-1-een en cyclohexaan hebben de volgende structuurformules:
Ringstructuur
[bewerken | brontekst bewerken]Een ringstructuur kan plat of in perspectief als een stoel worden getekend.
- Molecuulstructuur van cellobiose in perspectief
- Molecuulstructuur van cellobiose in de stoelconfiguratie
- Structuurformule van fructose in plat vlak weergegeven
Verschillende weergaven
[bewerken | brontekst bewerken]- ↑ YouTube. Molecuulformules en structuurformules. examenoverzicht.
- ↑ Nomenclature of inorganic chemistry: IUPAC recommendations 2005. Royal society of chemistry, Cambridge (2005). ISBN 978-0-85404-438-2.
- ↑ (en) Chemistry (IUPAC), The International Union of Pure and Applied, IUPAC - structural formula (S06061). goldbook.iupac.org. Geraadpleegd op 26 december 2025.