교차 결합 반응
유기화학에서 교차 결합 반응(영어: Cross-coupling reaction)은 두 개의 다른 단편이 결합하는 화학 반응이다. 교차 결합은 더 일반적인 짝지음 반응의 하위 집합이다. 종종 교차 결합 반응은 금속 촉매를 필요로 한다. 한 가지 중요한 반응 유형은 다음과 같다.
이러한 반응은 탄소-탄소 결합을 형성하는 데 사용될 뿐만 아니라 탄소-헤테로원자 결합을 형성하는 데도 사용된다.[1][2][3][4] 교차 결합 반응은 짝지음 반응의 하위 집합이다.
리처드 F. 헥, 네기시 에이이치, 그리고 스즈키 아키라는 팔라듐 촉매 짝지음 반응 개발로 2010년 노벨 화학상을 수상했다.[5][6]
반응 과정
[편집]금속 촉매를 필요로 하지 않는 반응을 포함하여 다양한 유형의 교차 결합을 반영하는 많은 반응 과정이 존재한다.[7] 그러나 종종 교차 결합은 친핵성 파트너와 친전자성 파트너의 금속 촉매 반응을 의미한다.
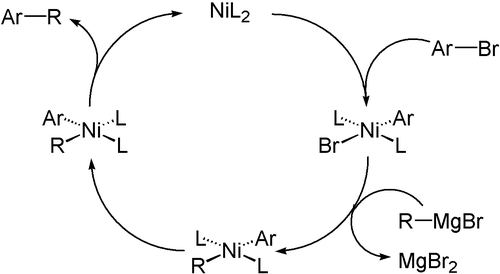
이러한 경우, 반응 과정은 일반적으로 LnMR(R') (L = 관중 리간드)로부터 R-R'의 환원적 제거를 포함한다. 이 중간체 LnMR(R')는 낮은 원자가 전구체 LnM으로부터 2단계 과정으로 형성된다. 유기 할로젠화물(RX)의 LnM에 대한 산화성 첨가는 LnMR(X)를 생성한다. 이어서 두 번째 파트너는 R'−의 공급원과 전이 금속화를 거친다. 마지막 단계는 두 개의 짝지음 조각의 환원적 제거이며, 이는 촉매를 재생성하고 유기 생성물을 생성한다. C(sp)−X 및 C(sp2)−X 결합과 같은 불포화 기질은 부분적으로 촉매에 쉽게 첨가되기 때문에 더 쉽게 짝지어진다.
촉매
[편집]
촉매는 종종 팔라듐을 기반으로 하는데, 이는 높은 작용기 내성으로 인해 자주 선택된다. 유기 팔라듐 화합물은 일반적으로 물과 공기에 대해 안정적이다. 팔라듐 촉매는 중금속에 대한 광범위한 규제를 직면하고 있는 제약 산업에 문제가 될 수 있다. 많은 제약 화학자들은 제품 내 금속 흔적을 최소화하기 위해 생산 초기에 짝지음 반응을 사용하려고 한다.[8] Pd 기반의 불균일 촉매도 잘 개발되어 있다.[9]
구리 기반 촉매도 흔하며, 특히 헤테로원자-탄소 결합을 포함하는 짝지음 반응에 사용된다.[10][11]
철-,[12] 코발트-,[13] 니켈 기반[14] 촉매도 연구되었다.
이탈기
[편집]유기 파트너의 이탈기 X는 일반적으로 할로젠화물이지만, 트라이플레이트, 토실레이트, 피발레이트 에스터 및 기타 유사할로젠화물이 사용되었다.[15] 염화물은 유기염소 화합물의 저렴한 비용 때문에 이상적인 그룹이다. 그러나 종종 C-Cl 결합은 너무 불활성하여 허용 가능한 반응 속도를 위해 브로민화물 또는 아이오딘화물 이탈기가 필요하다. 유기금속 파트너의 주족 금속은 일반적으로 주석 (원소), 아연, 규소 또는 붕소와 같은 전기양성 원소이다.
탄소–탄소 교차 결합
[편집]많은 교차 결합은 탄소-탄소 결합 형성을 포함한다.
| 반응 | 년도 | 반응물 A | 반응물 B | 촉매 | 비고 | ||
|---|---|---|---|---|---|---|---|
| 카디오-초드키에비츠 반응 | 1957 | RC≡CH | sp | RC≡CX | sp | Cu | 염기 필요 |
| 카스트로-스테판스 반응 | 1963 | RC≡CH | sp | Ar-X | sp2 | Cu | |
| 코리–하우스 합성 | 1967 | R2CuLi 또는 RMgX | sp3 | R-X | sp2, sp3 | Cu | 1971년 제이 코치에 의한 구리 촉매 버전 |
| 구마다 반응 | 1972 | RMgBr | sp2, sp3 | R-X | sp2 | Pd 또는 Ni 또는 Fe | |
| 헥 반응 | 1972 | 알켄 | sp2 | Ar-X | sp2 | Pd 또는 Ni | 염기 필요 |
| 소노가시라 반응 | 1975 | ArC≡CH | sp | R-X | sp3 sp2 | Pd 및 Cu | 염기 필요 |
| 네기시 반응 | 1977 | R-Zn-X | sp3, sp2, sp | R-X | sp3 sp2 | Pd 또는 Ni | |
| 스틸 커플링 | 1978 | R-SnR3 | sp3, sp2, sp | R-X | sp3 sp2 | Pd 또는 Ni | |
| 스즈키-미야우라 반응 | 1979 | R-B(OR)2 | sp2 | R-X | sp3 sp2 | Pd 또는 Ni | 염기 필요 |
| 무라하시 반응[16] | 1979 | R-Li | sp2, sp3 | R-X | sp2 | Pd 또는 Ru | |
| 히야마 반응 | 1988 | R-SiR3 | sp2 | R-X | sp3 sp2 | Pd | 염기 필요 |
| 후쿠야마 반응 | 1998 | R-Zn-I | sp3 | RCO(SEt) | sp2 | Pd 또는 Ni | 리베스킨드-스로글 커플링 참조, 케톤 생성 |
| 리베스킨드-스로글 반응 | 2000 | R-B(OR)2 | sp3, sp2 | RCO(SEt) Ar-SMe | sp2 | Pd | CuTC 필요, 케톤 생성 |
| 교차 탈수소 반응 | 2004 | R-H | sp, sp2, sp3 | R'-H | sp, sp2, sp3 | Cu, Fe, Pd 등 | 산화제 또는 탈수소 필요 |
| 탈카복실화 교차 결합 | 2000년대 | R-CO2H | sp2 | R'-X | sp, sp2 | Cu, Pd | 염기가 거의 또는 전혀 필요 없음 |
탄소 원자 기하학에 대한 제약은 촉매와 착화될 때 주로 β-수소화물 제거를 억제한다.[17]
탄소–헤테로원자 결합
[편집]많은 교차 결합은 탄소-헤테로원자 (헤테로원자 = S, N, O) 결합 형성을 포함한다. 인기 있는 방법은 부흐발트-하트위그 반응이다.
-
(Eq.1)
| 반응 | 년도 | 반응물 A | 반응물 B | 촉매 | 비고 | ||
|---|---|---|---|---|---|---|---|
| 울만형 반응 | 1905 | ArO-MM, ArNH2,RS-M,NC-M | sp3 | Ar-X (X = OAr, N(H)Ar, SR, CN) | sp2 | Cu | |
| 부흐발트-하트위그 반응[18] | 1994 | R2N-H | sp3 | R-X | sp2 | Pd | N-C 커플링, 2세대 자유 아민 |
| 찬–람 반응[19] | 1998 | Ar-B(OR)2 | sp2 | Ar-NH2 | sp2 | Cu | |
기타 반응
[편집]팔라듐은 할로젠화 아렌과 플루오린화 아렌의 교차 결합을 촉매한다. 이 과정은 C–H 기능화를 통해 전자가 부족한 아렌에서 일어난다는 점에서 특이하다.[20]
응용
[편집]교차 결합 반응은 몬테루카스트, 엘레트립탄, 나프록센, 바레니클린, 그리고 레스베라트롤과 같은 의약품 생산에 중요하다.[4][21] 스즈키-미야우라 반응이 가장 널리 사용된다.[22] 일부 중합체와 단량체도 이러한 방식으로 제조된다.[23]
문헌
[편집]- Fortman, George C.; Nolan, Steven P. (2011). 《N-Heterocyclic carbene (NHC) ligands and palladium in homogeneous cross-coupling catalysis: a perfect union》 (영어). 《Chemical Society Reviews》 40. 5151–69쪽. doi:10.1039/c1cs15088j. PMID 21731956.
- Yin; Liebscher, Jürgen (2007). 《Carbon−Carbon Coupling Reactions Catalyzed by Heterogeneous Palladium Catalysts》. 《Chemical Reviews》 107. 133–173쪽. doi:10.1021/cr0505674. PMID 17212474. S2CID 36974481.
- Jana, Ranjan; Pathak, Tejas P.; Sigman, Matthew S. (2011). 《Advances in Transition Metal (Pd,Ni,Fe)-Catalyzed Cross-Coupling Reactions Using Alkyl-organometallics as Reaction Partners》. 《Chemical Reviews》 111. 1417–1492쪽. doi:10.1021/cr100327p. PMC 3075866. PMID 21319862.
- Molnár, Árpád (2011). 《Efficient, Selective, and Recyclable Palladium Catalysts in Carbon−Carbon Coupling Reactions》. 《Chemical Reviews》 111. 2251–2320쪽. doi:10.1021/cr100355b. PMID 21391571.
- Miyaura, Norio; Suzuki, Akira (1995). 《Palladium-Catalyzed Cross-Coupling Reactions of Organoboron Compounds》. 《Chemical Reviews》 95. 2457–2483쪽. CiteSeerX 10.1.1.735.7660. doi:10.1021/cr00039a007.
- Roglans, Anna; Pla-Quintana, Anna; Moreno-Mañas, Marcial (2006). 《Diazonium Salts as Substrates in Palladium-Catalyzed Cross-Coupling Reactions》. 《Chemical Reviews》 106. 4622–4643쪽. doi:10.1021/cr0509861. PMID 17091930. S2CID 8128630.
- Korch, Katerina M.; Watson, Donald A. (2019). 《Cross-Coupling of Heteroatomic Electrophiles》. 《Chemical Reviews》 119. 8192–8228쪽. doi:10.1021/acs.chemrev.8b00628. PMC 6620169. PMID 31184483.
- Cahiez, Gérard; Moyeux, Alban (2010). 《Cobalt-Catalyzed Cross-Coupling Reactions》. 《Chemical Reviews》 110. 1435–1462쪽. doi:10.1021/cr9000786. PMID 20148539.
- Yi, Hong; Zhang, Guoting; Wang, Huamin; Huang, Zhiyuan; Wang, Jue; Singh, Atul K.; Lei, Aiwen (2017). 《Recent Advances in Radical C–H Activation/Radical Cross-Coupling》. 《Chemical Reviews》 117. 9016–9085쪽. doi:10.1021/acs.chemrev.6b00620. PMID 28639787.
각주
[편집]- ↑ Korch, Katerina M.; Watson, Donald A. (2019). 《Cross-Coupling of Heteroatomic Electrophiles》. 《Chemical Reviews》 119. 8192–8228쪽. doi:10.1021/acs.chemrev.8b00628. PMC 6620169. PMID 31184483.
- ↑ Corbet, Jean-Pierre; Mignani, Gérard (2006). 《Selected Patented Cross-Coupling Reaction Technologies》. 《Chemical Reviews》 106. 2651–2710쪽. doi:10.1021/cr0505268. PMID 16836296.
- ↑ New Trends in Cross-Coupling: Theory and Applications Thomas Colacot (Editor) 2014 ISBN 978-1-84973-896-5
- ↑ 가 나 King, A. O.; Yasuda, N. (2004). 〈Palladium-Catalyzed Cross-Coupling Reactions in the Synthesis of Pharmaceuticals〉. 《Organometallics in Process Chemistry》. Topics in Organometallic Chemistry 6. Heidelberg: Springer. 205–245쪽. doi:10.1007/b94551. ISBN 978-3-540-01603-8.
- ↑ “The Nobel Prize in Chemistry 2010 - Richard F. Heck, Ei-ichi Negishi, Akira Suzuki”. NobelPrize.org. 2010년 10월 6일. 2010년 10월 6일에 확인함.
- ↑ Johansson Seechurn, Carin C. C.; Kitching, Matthew O.; Colacot, Thomas J.; Snieckus, Victor (2012). 《Palladium-Catalyzed Cross-Coupling: A Historical Contextual Perspective to the 2010 Nobel Prize》. 《Angewandte Chemie International Edition》 51. 5062–5085쪽. doi:10.1002/anie.201107017. PMID 22573393. S2CID 20582425.
- ↑ Sun, Chang-Liang; Shi, Zhang-Jie (2014). 《Transition-Metal-Free Coupling Reactions》. 《Chemical Reviews》 114. 9219–9280쪽. doi:10.1021/cr400274j. PMID 25184859.
- ↑ Thayer, Ann (2005년 9월 5일). 《Removing Impurities》. 《Chemical & Engineering News》. 2015년 12월 11일에 확인함.
- ↑ Yin, L.; Liebscher, J. (2007). 《Carbon−Carbon Coupling Reactions Catalyzed by Heterogeneous Palladium Catalysts》. 《Chemical Reviews》 107. 133–173쪽. doi:10.1021/cr0505674. PMID 17212474. S2CID 36974481.
- ↑ Corbet, Jean-Pierre; Mignani, Gérard (2006). 《Selected Patented Cross-Coupling Reaction Technologies》. 《Chemical Reviews》 106. 2651–2710쪽. doi:10.1021/cr0505268. PMID 16836296.
- ↑ Evano, Gwilherm; Blanchard, Nicolas; Toumi, Mathieu (2008). 《Copper-Mediated Coupling Reactions and Their Applications in Natural Products and Designed Biomolecules Synthesis》. 《Chemical Reviews》 108. 3054–3131쪽. doi:10.1021/cr8002505. PMID 18698737.
- ↑ Robin B. Bedford (2015). 《How Low Does Iron Go? Chasing the Active Species in Fe-Catalyzed Cross-Coupling Reactions》. 《Acc. Chem. Res.》 48. 1485–1493쪽. doi:10.1021/acs.accounts.5b00042. PMID 25916260.
- ↑ Cahiez, GéRard; Moyeux, Alban (2010). 《Cobalt-Catalyzed Cross-Coupling Reactions》. 《Chemical Reviews》 110. 1435–1462쪽. doi:10.1021/cr9000786. PMID 20148539.
- ↑ Rosen, Brad M.; Quasdorf, Kyle W.; Wilson, Daniella A.; Zhang, Na; Resmerita, Ana-Maria; Garg, Neil K.; Percec, Virgil (2011). 《Nickel-Catalyzed Cross-Couplings Involving Carbon−Oxygen Bonds》. 《Chemical Reviews》 111. 1346–1416쪽. doi:10.1021/cr100259t. PMC 3055945. PMID 21133429.
- ↑ Smith, Michael B.; March, Jerry (2007), 《Advanced Organic Chemistry: Reactions, Mechanisms, and Structure》 6판, New York: Wiley-Interscience, 792쪽, ISBN 978-0-471-72091-1
- ↑ Murahashi, Shunichi; Yamamura, Masaaki; Yanagisawa, Kenichi; Mita, Nobuaki; Kondo, Kaoru (1979). 《Stereoselective synthesis of alkenes and alkenyl sulfides from alkenyl halides using palladium and ruthenium catalysts》 (영어). 《The Journal of Organic Chemistry》 44. 2408–2417쪽. doi:10.1021/jo01328a016. ISSN 0022-3263.
- ↑ Clayden, J.; Greeves, N.; Warren, S. Organic Chemistry, 2nd ed.; Oxford UP: Oxford, U.K., 2012. pp. 1069-1102.
- ↑ Ruiz-Castillo, P.; Buchwald, S. L. (2016). 《Applications of Palladium-Catalyzed C–N Cross-Coupling Reactions》. 《Chemical Reviews》 116. 12564–12649쪽. doi:10.1021/acs.chemrev.6b00512. PMC 5070552. PMID 27689804.
- ↑ Jennifer X. Qiao; Patrick Y.S. Lam (2011). 〈Recent Advances in Chan–Lam Coupling Reaction: Copper-Promoted C–Heteroatom Bond Cross-Coupling Reactions with Boronic Acids and Derivatives〉. Dennis G. Hall (편집). 《Boronic Acids: Preparation and Applications in Organic Synthesis, Medicine and Materials》. Wiley-VCH. 315–361쪽. doi:10.1002/9783527639328.ch6. ISBN 9783527639328.
- ↑ M. Lafrance; C. N. Rowley; T. K. Woo; K. Fagnou (2006). 《Catalytic Intermolecular Direct Arylation of Perfluorobenzenes》. 《J. Am. Chem. Soc.》 128. 8754–8756쪽. Bibcode:2006JAChS.128.8754L. CiteSeerX 10.1.1.631.607. doi:10.1021/ja062509l. PMID 16819868.
- ↑ Cornils, Boy; Börner, Armin; Franke, Robert; Zhang, Baoxin; Wiebus, Ernst; Schmid, Klaus (2017). 〈Hydroformylation〉. 《Applied Homogeneous Catalysis with Organometallic Compounds》. 23–90쪽. doi:10.1002/9783527651733.ch2. ISBN 9783527328970.
- ↑ Roughley, Stephen D.; Jordan, Allan M. (2011). 《The Medicinal Chemist's Toolbox: An Analysis of Reactions Used in the Pursuit of Drug Candidates》. 《Journal of Medicinal Chemistry》 54. 3451–3479쪽. doi:10.1021/jm200187y. PMID 21504168.
- ↑ Hartwig, J. F. Organotransition Metal Chemistry, from Bonding to Catalysis; University Science Books: New York, 2010. ISBN 1-891389-53-X


